COVID కోసం ఫైజర్ యొక్క mRNA వ్యాక్సిన్ రిబోన్యూక్లియిక్ యాసిడ్ (RNA)ని చికిత్సా లక్ష్యంగా ఉపయోగించాలనే అభిరుచిని పుంజుకుంది.అయినప్పటికీ, చిన్న అణువులతో RNAని లక్ష్యంగా చేసుకోవడం చాలా సవాలుతో కూడుకున్నది.
RNAలో నాలుగు బిల్డింగ్ బ్లాక్లు మాత్రమే ఉన్నాయి: అడెనిన్ (A), సైటోసిన్ (C), గ్వానైన్ (G), మరియు యురేసిల్ (U) ఇవి DNAలో కనిపించే థైమిన్ (T)ని భర్తీ చేస్తాయి.ఇది ఔషధ ఎంపికను దాదాపు అధిగమించలేని అడ్డంకిగా చేస్తుంది.దీనికి విరుద్ధంగా, ప్రోటీన్లను తయారు చేసే 22 సహజ అమైనో ఆమ్లాలు ఉన్నాయి, ఇది చాలా ప్రోటీన్-టార్గెటింగ్ డ్రగ్స్ సాపేక్షంగా మంచి ఎంపికను ఎందుకు కలిగి ఉందో వివరిస్తుంది.
RNA యొక్క నిర్మాణం మరియు పనితీరు
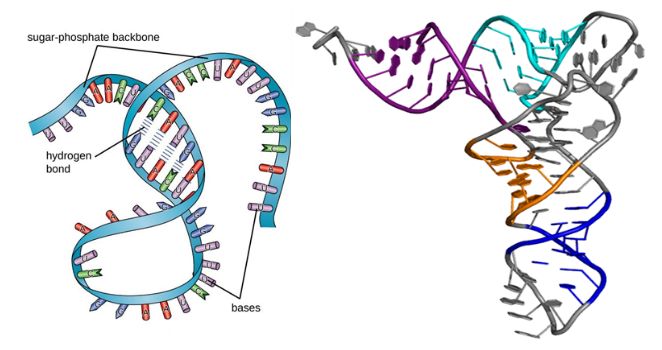
ప్రోటీన్ల వలె, RNA అణువులు క్రింది చిత్రంలో చూపిన విధంగా ద్వితీయ మరియు తృతీయ నిర్మాణాలను కలిగి ఉంటాయి.అవి సింగిల్-చైన్ స్థూల కణములు అయినప్పటికీ, బేస్ జత చేయడం వల్ల ఉబ్బెత్తులు, లూప్లు మరియు హెలిక్స్లు ఏర్పడినప్పుడు వాటి ద్వితీయ నిర్మాణం ఆకారంలోకి వస్తుంది.అప్పుడు, త్రిమితీయ మడత RNA యొక్క తృతీయ నిర్మాణానికి దారి తీస్తుంది, ఇది దాని స్థిరత్వం మరియు పనితీరుకు అవసరం.
మూర్తి 1. RNA యొక్క నిర్మాణం
RNAలో మూడు రకాలు ఉన్నాయి:
- మెసెంజర్ RNA (mRNA)DNA నుండి జన్యు సమాచారాన్ని లిప్యంతరీకరించడం మరియు రైబోజోమ్పై ఒక బేస్ సీక్వెన్స్గా బదిలీ చేయబడుతుంది;ఎల్
- రైబోసోమల్ RNA (rRNA)రైబోజోమ్లు అని పిలువబడే ప్రోటీన్-సింథసైజింగ్ ఆర్గానిల్స్లో భాగం, ఇవి సైటోప్లాజమ్కు ఎగుమతి చేయబడతాయి మరియు mRNAలోని సమాచారాన్ని ప్రోటీన్లుగా అనువదించడంలో సహాయపడతాయి;
- బదిలీ RNA (tRNA)mRNA మరియు ప్రోటీన్ను రూపొందించే అమైనో ఆమ్ల గొలుసు మధ్య లింక్.
ఆర్ఎన్ఏను చికిత్సా లక్ష్యంగా లక్ష్యంగా చేసుకోవడం చాలా ఆకర్షణీయంగా ఉంటుంది.మన జన్యువులో కేవలం 1.5% మాత్రమే ప్రోటీన్లోకి అనువదించబడిందని, 70%-90% RNAలోకి లిప్యంతరీకరించబడిందని కనుగొనబడింది.RNA అణువులు అన్ని జీవులకు అత్యంత ముఖ్యమైనవి.ఫ్రాన్సిస్ క్రిక్ యొక్క “సెంట్రల్ డాగ్మా” ప్రకారం, DNA నుండి జన్యు సమాచారాన్ని ప్రోటీన్లలోకి అనువదించడం RNA యొక్క అత్యంత కీలకమైన పాత్ర.అంతేకాకుండా, RNA అణువులకు ఇతర విధులు కూడా ఉన్నాయి, వీటిలో:
- ప్రోటీన్ సంశ్లేషణలో అడాప్టర్ అణువుల వలె పనిచేస్తుంది;ఎల్
- DNA మరియు రైబోజోమ్ల మధ్య దూతగా పనిచేస్తోంది;ఎల్
- అవి అన్ని జీవ కణాలలో జన్యు సమాచారం యొక్క వాహకాలు;ఎల్
- కొత్త ప్రోటీన్లను సంశ్లేషణ చేయడానికి అవసరమైన సరైన అమైనో ఆమ్లాల రైబోసోమల్ ఎంపికను ప్రోత్సహించడంవివో లో.
యాంటీబయాటిక్స్
1940ల నాటికే కనుగొనబడినప్పటికీ, అనేక యాంటీబయాటిక్ల చర్య యొక్క విధానం 1980ల చివరి వరకు విశదీకరించబడలేదు.యాంటీబయాటిక్స్లో ఎక్కువ భాగం బ్యాక్టీరియా రైబోజోమ్లతో బంధించడం ద్వారా తగిన ప్రొటీన్లను తయారు చేయకుండా నిరోధించడం ద్వారా బ్యాక్టీరియాను చంపేస్తుందని కనుగొనబడింది.
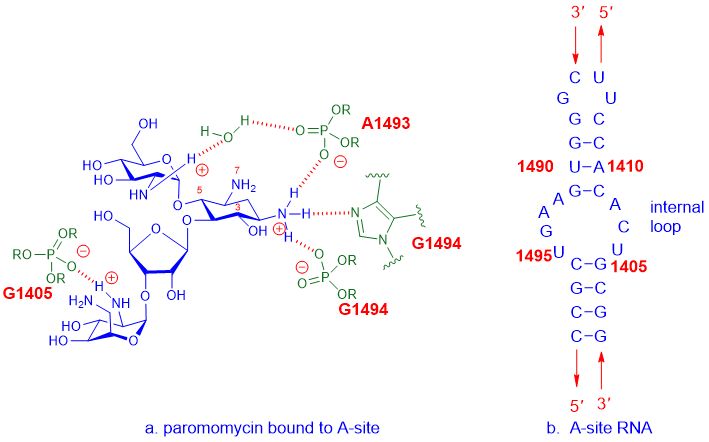
ఉదాహరణకు, అమినోగ్లైకోసైడ్ యాంటీబయాటిక్స్ 30S రైబోజోమ్ సబ్యూనిట్లో భాగమైన 16S rRNA యొక్క A-సైట్తో బంధిస్తుంది, ఆపై బ్యాక్టీరియా పెరుగుదలకు ఆటంకం కలిగించడానికి ప్రోటీన్ సంశ్లేషణలో జోక్యం చేసుకుంటుంది, చివరికి కణాల మరణానికి దారితీస్తుంది.A-సైట్ అమినోఅసిల్ సైట్ను సూచిస్తుంది, దీనిని tRNA అంగీకరించే సైట్ అని కూడా పిలుస్తారు.వంటి అమినోగ్లైకోసైడ్ ఔషధాల మధ్య వివరణాత్మక పరస్పర చర్యపరోమోమైసిన్, మరియు A-సైట్E. కోలిRNA క్రింద చూపబడింది.
మూర్తి 2. పారోమోమైసిన్ మరియు A-సైట్ మధ్య పరస్పర చర్యE. కోలిRNA
దురదృష్టవశాత్తూ, అమినోగ్లైకోసైడ్ ఔషధాలతో సహా అనేక A-సైట్ ఇన్హిబిటర్లు, నెఫ్రోటాక్సిసిటీ, డోస్-డిపెండెంట్ మరియు నిర్దిష్ట కోలుకోలేని ఓటోటాక్సిసిటీ వంటి భద్రతా సమస్యలను కలిగి ఉన్నాయి.RNA చిన్న అణువులను గుర్తించడానికి అమినోగ్లైకోసైడ్ ఔషధాలలో ఎంపిక లేకపోవడం వల్ల ఈ విషపూరితం ఏర్పడింది.
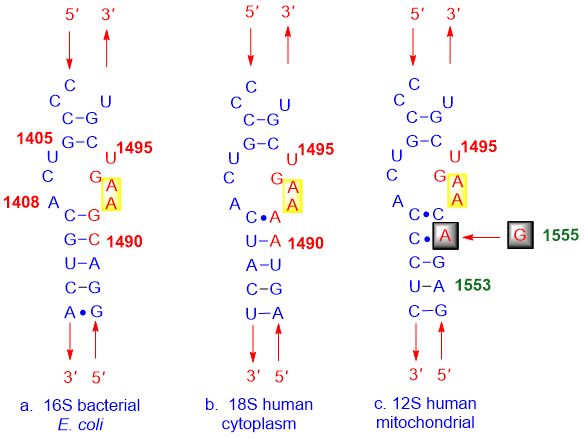
దిగువ చిత్రంలో చూపిన విధంగా: (a) బ్యాక్టీరియా యొక్క నిర్మాణం, (b) మానవ కణ త్వచం మరియు (c) మానవ మైటోకాన్డ్రియల్ A- సైట్ చాలా పోలి ఉంటాయి, A- సైట్ నిరోధకాలు వాటన్నింటికీ కట్టుబడి ఉంటాయి.
మూర్తి 3. నాన్-సెలెక్టివ్ A-సైట్ ఇన్హిబిటర్ బైండింగ్
టెట్రాసైక్లిన్ యాంటీబయాటిక్స్ కూడా rRNA యొక్క A-సైట్ను నిరోధిస్తాయి.Mgతో సంక్లిష్టమైన 30S సబ్యూనిట్లోని హెలికల్ రీజియన్ (H34)కి రివర్స్గా బైండింగ్ చేయడం ద్వారా బ్యాక్టీరియా ప్రోటీన్ సంశ్లేషణను అవి ఎంపిక చేసి నిరోధిస్తాయి.2+.
మరోవైపు, మాక్రోలైడ్ యాంటీబయాటిక్స్ నాసెంట్ పెప్టైడ్స్ (NPET) కోసం బ్యాక్టీరియా రైబోజోమ్ టన్నెల్ యొక్క నిష్క్రమణ సైట్ (E-సైట్) దగ్గర బంధిస్తుంది మరియు దానిని పాక్షికంగా అడ్డుకుంటుంది, తద్వారా బ్యాక్టీరియా ప్రోటీన్ సంశ్లేషణను నిరోధిస్తుంది.చివరగా, ఆక్సాజోలిడినోన్ యాంటీబయాటిక్స్ వంటివిలైన్జోలిడ్(Zyvox) బ్యాక్టీరియా 50S రైబోసోమల్ సబ్యూనిట్లో లోతైన చీలికతో బంధిస్తుంది, దీని చుట్టూ 23S rRNA న్యూక్లియోటైడ్లు ఉంటాయి.
యాంటిసెన్స్ ఒలిగోన్యూక్లియోటైడ్స్ (ASO)
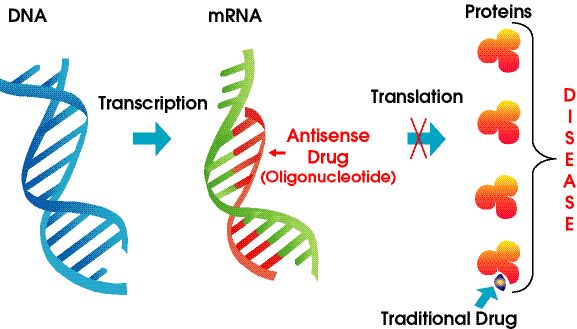
యాంటిసెన్స్ డ్రగ్స్ రసాయన-మార్పు చేసిన న్యూక్లియిక్ యాసిడ్ పాలిమర్లు, ఇవి RNAని లక్ష్యంగా చేసుకుంటాయి.వారు MRNAని లక్ష్యంగా చేసుకోవడానికి వాట్సన్-క్రిక్ బేస్ జత చేయడంపై ఆధారపడతారు, ఫలితంగా జన్యు నిశ్శబ్దం, స్టెరిక్ దిగ్బంధనం లేదా స్ప్లికింగ్ మార్పు ఏర్పడుతుంది.ASOలు సెల్ న్యూక్లియస్లోని ప్రీ-ఆర్ఎన్ఏలతో మరియు సైటోప్లాజంలోని పరిపక్వ mRNAలతో సంకర్షణ చెందుతాయి.వారు ఎక్సోన్లు, ఇంట్రాన్లు మరియు అనువదించని ప్రాంతాలను (UTRలు) లక్ష్యంగా చేసుకోవచ్చు.ఈ రోజు వరకు, డజనుకు పైగా ASO మందులు FDAచే ఆమోదించబడ్డాయి.
మూర్తి 4. యాంటిసెన్స్ టెక్నాలజీ
ఆర్ఎన్ఏ లక్ష్యంగా చిన్న మాలిక్యూల్ డ్రగ్స్
2015లో, నోవార్టిస్ వారు బ్రానాప్లామ్ అని పిలువబడే SMN2 స్ప్లికింగ్ రెగ్యులేటర్ను కనుగొన్నారని నివేదించారు, ఇది U1-ప్రీ-mRNA యొక్క అనుబంధాన్ని పెంచుతుంది మరియు SMA ఎలుకలను కాపాడుతుంది.
మరోవైపు, SMA చికిత్స కోసం 2020లో FDAచే PTC/రోచెస్ రిస్డిప్లామ్ (ఎవ్రిస్డి) ఆమోదించబడింది.బ్రానాప్లామ్ లాగా, రిస్డిప్లామ్ కూడా ఫంక్షనల్ SMN ప్రోటీన్లను ఉత్పత్తి చేయడానికి సంబంధిత SMN2 జన్యువుల విభజనను నియంత్రించడం ద్వారా పనిచేస్తుంది.
RNA డిగ్రేడర్లు
RBM అంటే RNA-బైండింగ్ మోటిఫ్ ప్రోటీన్.ముఖ్యంగా, ఇండోల్ సల్ఫోనామైడ్ ఒక పరమాణు అంటుకునేది.ఇది RBM39ని CRL4-DCAF15 E3 ubiquitin ligaseకి ఎంపిక చేసి, RBM39 పాలీయుబిక్విటేషన్ మరియు ప్రోటీన్ డిగ్రేడేషన్ను ప్రోత్సహిస్తుంది.జన్యుపరమైన క్షీణత లేదా RBM39 యొక్క సల్ఫోనామైడ్-మధ్యవర్తిత్వ క్షీణత ముఖ్యమైన జన్యు-వ్యాప్త స్ప్లికింగ్ అసాధారణతలను ప్రేరేపిస్తుంది, చివరికి కణాల మరణానికి దారితీస్తుంది.
RNA-PROTACలు RNA-బైండింగ్ ప్రోటీన్లను (RBPs) క్షీణింపజేయడానికి అభివృద్ధి చేయబడ్డాయి.PROTAC E3 లిగేస్ లిగాండ్ను RNA లిగాండ్కు కనెక్ట్ చేయడానికి లింకర్ను ఉపయోగిస్తుంది, ఇది RNA మరియు RBPలకు బంధిస్తుంది.RBP నిర్దిష్ట ఒలిగోన్యూక్లియోటైడ్ సీక్వెన్స్లకు కట్టుబడి ఉండే స్ట్రక్చరల్ డొమైన్లను కలిగి ఉన్నందున, RNA-PROTAC ఒలిగోన్యూక్లియోటైడ్ క్రమాన్ని ఆసక్తి ప్రోటీన్ (POI) కోసం లిగాండ్గా ఉపయోగిస్తుంది.అంతిమ ఫలితం RBPల క్షీణత.
ఇటీవల, స్క్రిప్స్ ఇన్స్టిట్యూషన్ ఆఫ్ ఓషనోగ్రఫీకి చెందిన ప్రొఫెసర్ మాథ్యూ డిస్నీ RNAను కనుగొన్నారు.రిబోన్యూక్లీస్-టార్గెటింగ్ చిమెరాస్ (RiboTACs).RiboTAC అనేది RNase L లిగాండ్ మరియు RNA లిగాండ్ను లింకర్తో అనుసంధానించే ఒక హెటెరోఫంక్షనల్ మాలిక్యూల్.ఇది నిర్దిష్ట RNA లక్ష్యాలకు అంతర్జాత RNase Lని ప్రత్యేకంగా నియమించగలదు, ఆపై సెల్యులార్ న్యూక్లియిక్ యాసిడ్ బ్రేక్డౌన్ మెకానిజం (RNase L)ని ఉపయోగించి RNAను విజయవంతంగా తొలగించగలదు.
పరిశోధకులు చిన్న అణువులు మరియు RNA లక్ష్యాల మధ్య పరస్పర చర్య గురించి మరింత తెలుసుకున్నందున, ఈ పద్ధతిని ఉపయోగించి మరిన్ని మందులు భవిష్యత్తులో ఉద్భవించాయి.
పోస్ట్ సమయం: ఆగస్ట్-02-2023